El estudio EUSTAR (European League Against Rheumatism Scleroderma Trial and Research) sobre una población de 3656 pacientes con esclerosis sistémica (ES) reveló enfermedad pulmonar intersticial en el 53% de aquellos con enfermedad cutánea difusa y en el 35% de los afectados por ES limitada a la piel. La enfermedad pulmonar intersticial (EPI) ocupa, junto con la hipertensión pulmonar, el primer lugar como causa de muerte en estos pacientes. Son puntos clave a la hora de indicar el tratamiento la identificación de pacientes con riesgo de progresión de la EPI (Tabla 1) la determinación de la extensión de la enfermedad (Tabla 2) y sus posibilidades de respuesta (Tabla 3)
|
Tabla 1: Riesgo de progresión de la enfermedad pulmonar intersticial asociada a esclerodermia
|
EPI : enfermedad pulmonar intersticial; ES: esclerosis sistémica; FVC: capacidad vital forzada; HRCT: tomografía computada de alta resolución
Tabla 2: Determinación de la extensión de enfermedad pulmonar intersticial asociada a esclerodermia
|
|
Extensa |
Limitada |
|
Anormalidades HRCT |
>30% |
< 10% |
|
Pacientes con anormalidades HRCT <30% >10% |
||
|
FVC |
<70% |
>70% |
|
HRCT: tomografía computada de alta resolución; FVC: capacidad vital forzada |
||
|
Tabla 3: Factores asociados a respuesta terapéutica
HRCT tomografía computada de alta resolución; FVC: capacidad vital forzada |
Ante la ausencia de un tratamiento específico se ha sugerido que los inmunosupresores podrían aplicarse al tratamiento de la EPI asociada a ES. Después de analizar sendos estudios aleatorizados controlados, Scleroderma Lung Study I (Tashkin D., et al. NEJM., 2006) y Fibrosing Alveolitis in Scleroderma Trial (Nadashkevich O, et al. Clin Rheum 2006), expertos del EUSTAR recomiendan, en pacientes con riesgo de progresión, instituir un tratamiento de inducción con ciclofosfamida tan rápidamente como sea posible (Avouac J, et al., Ann Rheum Dis 2009); por vía oral o parenteral. El esquema en pulsos intermitentes por vía IV (0.5 2 g-m-2 durante 6 a 18 meses) es de preferencia por ser menos tóxico (Figura 1); una vez que se ha alcanzado la remisión se recomienda iniciar un tratamiento de mantenimiento. En pacientes con mala tolerancia ciclofosfamida ésta puede reemplazarse por micofenolato a razón de 2 gr/día que, por otra parte, es el inmunosupresor más usado en tratamientos de mantenimiento. Los ensayos clínicos realizados con azatioprina no han dado buenos resultados por lo que el EUSTAR desaconseja su uso como inductor. Por su parte, el uso de metotrexate queda limitado a la ES con compromiso únicamente cutáneo (Figura 1). Respecto de los corticoides, a pesar de los riesgos de crisis renales, se han visto mejorías estadísticamente significativas radiológicas y clínicas, con peoría de la función pulmonar al suspenderse su uso. En lo concerniente al rituximab, no hay hasta el momento ensayos clínicos que sustenten su indicación y; los inhibidores del TNF-alfa no han mostrado ser eficaces. El trasplante de células madre hematopoyéticas, precedida por una inmunosupresión intensiva con ciclofosfamida, se ha propuesto como tratamiento en los estadios iniciales de la ES cutánea difusa; el comité integrado por expertos del European Group for Blood and Marrow Transplantation y la EUSTAR hallaron una asociación entre el trasplante y una mejoría significativa del índice cutáneo de Rodnan (mRss), aunque sin efecto sobre la función pulmonar.
Figura 1: Algoritmo de manejo de enfermedad pulmonar intersticial asociada a esclerodermia
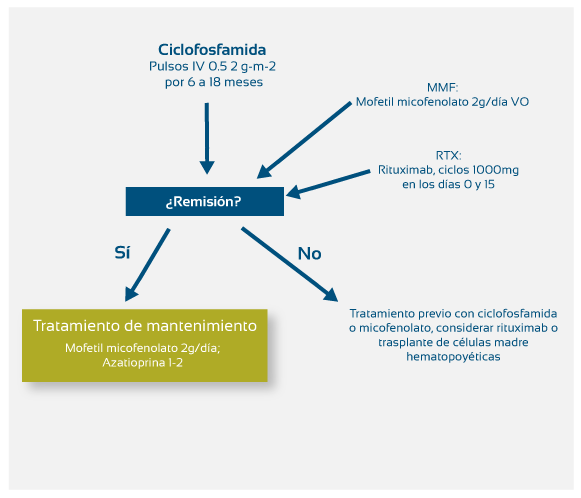
Los autores señalan que el monitoreo del tratamiento debe llevarse a cabo con tomografía computada de alta resolución y pruebas de función pulmonar, siendo recomendable contar con una evaluación subjetiva de la disnea.
Conclusión
Los autores concluyen que, aún en ausencia de indicadores de respuesta, la terapia inmunosupresora debe iniciarse tan rápidamente como sea posible ya que, si bien no está demostrado que se logre revertir la fibrosis ya instalada, contribuye a retrasar su progresión. Esta es la estrategia recomendada particularmente en aquellos pacientes con riesgo de progresión o función pulmonar más deteriorada.
 Acceso libre al artículo original
Acceso libre al artículo original
Susanna Cappelli, Serena Guiducci, Silvia Bellando Randone and Marco Matucci Cerinic. Immunosuppression for interstitial lung disease in systemic sclerosis. Eur Respir Rev 2013; 22: 236–243




